2. 自然资源部页岩气资源战略评价重点实验室, 北京 100083;
3. 筑波大学生命与环境学院, 日本 筑波市 305-0000;
4. 中国地质调查局油气资源调查中心, 北京 100083
2. Key Laboratory of Strategy Evaluation for Shale Gas, Ministry of Natural Resources, Beijing 100083 China;
3. Graduate School of Life and Environmental Sciences, University of Tsukuba, Tsukuba 305-0000, Japan;
4. Oil and Gas Resources Survey Center, China Geological Survey, Beijing 100083, China
[Objective] Framboidal pyrite are widespread in modern sediments and sedimentary rocks, widely considered organic or inorganic genesis. Although both formation mechanisms have theoretical and experimental support, a formation mechanism with general significance has not yet been established well. [Methods] This paper systematically and comprehensively studies the formation mechanism of framboidal pyrite, the application of redox conditions, and the influence of later environmental changes. [Results] The size and texture of pyrite framboids and the sulfur isotopes between framboids have fluctuated with the oxygen level. Therefore, framboidal pyrite is used as a reconstruct paleoenvironment proxy commonly. Although the microcrystallines of framboidal pyrite are correlated to the particle size positively, their (Morphological evolution sequence), growth patterns, (aggregation factors), as well as the relationship with paleo-redox are still poorly understood. The redox condition inverse from particle sizes of pyrite framboids and chromium reduction-determined sulfur isotope has certain limitations. Therefore, a comprehensive analysis of redox indicators is expected, which requiring further studies on links between in-situ sulfur isotope and particle sizes of framboidal pyrite. Although the framboidal surface chemistry can be modified as changes in late oxidation conditions, the size distribution of framboidal pyrite is still meaningful as a redox indicator. [Conclusions] In brief, experimental simulations, theoretical systems, and interdisciplinary studies on framboidal pyrite are still challenging and require further research.
从太古宙地层到现代海洋沉积物、从沉积岩到碳酸盐、从有机体到无机体、整个生物圈均发现黄铁矿的富集,尤其更常见于富有机质页岩(Steinike, 1963;Sawlowicz, 1993;Moore et al., 2009;Rickard, 2019)。黄铁矿的形态主要有草莓状、自形、充填和团块状等类型(Love et al., 1966),形态之间的差异反映了其形成过程水体物理化学条件与后期环境的不同(Wilkin et al., 1996;刘大猛等, 1999;Wei et al., 2016)。草莓状黄铁矿在沉积物和沉积岩中的普遍性,以及在反演古氧化-还原环境、确定矿床形成时间、成矿机制和生命起源等研究方面的重要意义(Sawlowicz, 1993),使其成为黄铁矿系列中研究的重点内容。
Rust(1935)对Ozark斜坡带矿物进行研究过程中,对草莓状黄铁矿结构进行了描述。此后不同的学者对草莓状黄铁矿的形成机制进行了研究(Kalliokoski et al., 1969;Horiuchi et al., 1974;Berner, 1984;Raiswell et al., 1985),尤其是Wilkin et al.(1996)对前人关于草莓状黄铁矿研究的总结以及对现代海洋沉积物中草莓状黄铁矿的大小、分布特征等方面进行的系统研究,奠定了草莓状黄铁矿的理论基础。在此基础之上,大量学者对草莓状黄铁矿及硫同位素分馏与古氧化-还原环境之间的关系进行了较为深入的研究,丰富了相关理论(Wignall et al., 1998;Farquhar et al., 2000;Farquhar et al., 2001;Bond et al., 2010)。与此同时,一系列模拟草莓状黄铁矿合成实验相继展开,对草莓状黄铁矿的无机成因机制进行研究,初步建立了草莓状黄铁矿理论体系(Morse et al., 1997; Ohfuji et al., 2005; Rickard, 2019)。
尽管国内外学者对草莓状黄铁矿进行了大量的研究,但是对一些基本问题的研究程度不够深入,例如压力在草莓状黄铁矿模拟实验中的效应、两种成因机制的界定及形成的草莓状黄铁矿的根本区别、粒径和微晶形态成因演化理论、反演古氧化-还原环境时存在局限性问题等。在对草莓状黄铁矿的形成机制、古氧化-还原环境反演及后期演化方面进行详细、全面论述的基础之上,对草莓状黄铁矿在模拟实验、理论体系和多学科交叉的研究进行展望,为下一步的研究方向提供参考。
2 草莓状黄铁矿的概念及形成机制 2.1 草莓状黄铁矿的概念草莓状黄铁矿是指由大小相近的具有似球-球状黄铁矿微晶聚集、堆积而成的球状集合体,主要成分为FeS2,微晶粒径为亚微米级别,具有离散、等维及等形的特征(图 1)(Rickard, 1970;Wilkin et al., 1996)。

|
图 1 扫描电镜下草莓状黄铁矿外形及微晶结构(据Ohfuji et al., 2005) (图c中箭头表示草莓状黄铁矿的微晶,具有离散、等维及等形的特征) Fig. 1 The shape and microcrystalline structure of framboidal pyrite under the scanning electron microscope(after Ohfuji et al., 2005) (The arrows in Fig.c show that the microcrystals of framboidal pyrite are discrete microcrystals, equidimensional and equimorphic) |
草莓状黄铁矿从有机成因→无机成因,尽管一直都是研究热点,但是许多假说、模型实验均是建立在一定的特殊条件之上,与实际形成环境存在一定的差异,尚未建立一种普遍的形成机制。总体上可以归结为有机成因和无机成因两种机制。
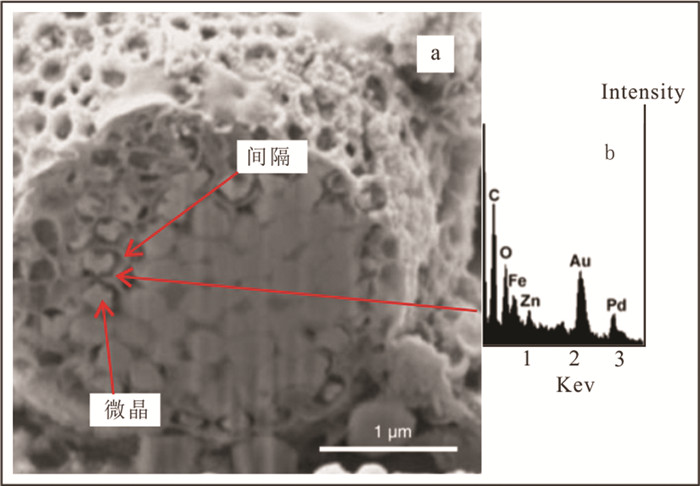
2.2.1 有机成因机制大量的研究表明草莓状黄铁矿的形成过程与有机质存在密切关系。这些关系体现在草莓状黄铁矿与生物颗粒外形和结构的相似性(Love, 1957;Kalliokoski et al., 1969)、细菌在草莓状黄铁矿形成过程中的作用(Berner, 1969;Lowenstam, 1981;Farina et al., 1990;Sawlowicz, 1993;Konhauser, 1997;Donald et al., 1999)、草莓状黄铁矿的富集与富有机质页岩中TOC良好的正相关关系(Sawlowicz, 1993;Bond et al., 2010;Wei et al., 2016; Zou et al., 2018)及其他星球潜在的生物标志化合物(Popa et al., 2004;MacLean et al., 2008),尤其是MacLean et al.(2008)提出一种草莓状黄铁矿的形成模式——“中空间隔”模式(图 2)。这些研究均为草莓状黄铁矿的有机成因机制提供了支撑。而Morse and Wang(1997)用冻干的浮游生物代替有机质进行了研究,表明黄铁矿形成速率大幅度(约20倍)降低,这与部分学者的研究结果是矛盾的,原因尚不清楚(Raiswell et al., 1985;Bond et al., 2010;Wei et al., 2016;Yang et al., 2016;Zou et al., 2018;Huang et al., 2019)。
|
图 2 “草莓状黄铁矿有机成因-中空间隔模式”(据MacLean et al., 2008修改) a—FIB技术对草莓状黄铁矿的横切面,可见微晶和“间隔”;b—通过能量色散X光谱,表示间隔中碳的富集 Fig. 2 Framboidal pyrite organic origin-"A hollow compartment"model (modified from MacLean et al., 2008) a-FIB-sectioned outer portion of this framboidal pyrite, found microcrystals and"compartment"; b-By energy dispersive X-ray indicating that the compartment is full with extensive carbon-rich |
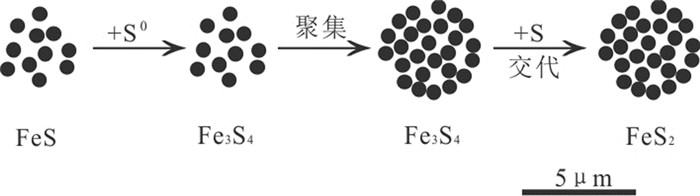
草莓状黄铁矿的一系列无机模拟实验,以及在生物数量不丰富的火山岩高温系统和热液体系的发现,为无机成因提供了支撑(Berner, 1969;Kalliokoski et al., 1969;Farrand, 1970;Sweeney et al., 1973;England et al., 1993;Wang et al., 1996;Morse et al., 1997;Wilkin et al., 1997a;Butler et al., 2000;Ohfuji et al., 2005)。Wilkin and Barnes(1997)认为草莓状黄铁矿的形成过程可以划分为4个连续阶段(图 3)(Wilkin et al., 1997a;杨雪英等, 2011):(1)初始单硫化铁微晶的形核和生长。(2)微晶之间的反应形成胶黄铁矿(Fe3S4)。(3)大小均匀的胶黄铁矿微晶在磁性作用下聚集生长。(4)胶黄铁矿由于交代作用形成草莓状黄铁矿。
|
图 3 Wilkin和Barnes关于草莓状黄铁矿形成的模式图(据Wilkin et al., 1996;杨雪英等,2011) Fig. 3 Wilkin and Barnes, sketch showing the forming process of framboidal pyrite (after Wilkin et al., 1996; Yang Xueying et al., 2011) |
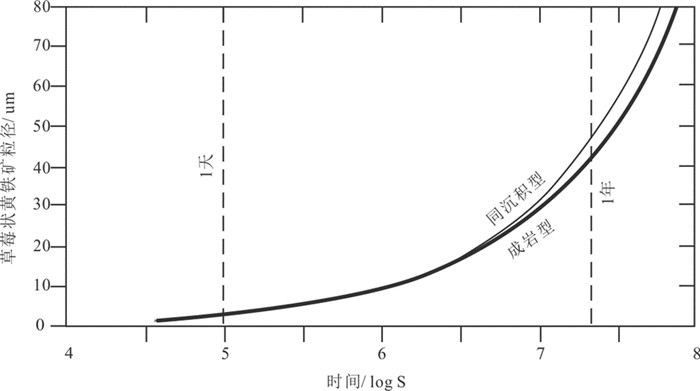
Ohfuji and Rickard(2005)认为无机合成草莓状黄铁矿的形成主要受控于溶液的pH值、硫化物浓度、氧化物、营养盐等因素,尤其是过饱和的黄铁矿浓度;Richard(2019)利用扩散-成核模型在无机环境下对草莓状黄铁矿形成的时间进行了模拟,结果表明成岩型草莓状黄铁矿平均形成时间约5 d,同沉积型草莓状黄铁矿平均形成时间3 d,而且两种类型的草莓状黄铁矿的形成时间和粒径成正比(图 4)。这个实验研究不仅为草莓状黄铁矿的无机形成机制提供支撑,也进一步为草莓状黄铁矿粒径大小与形成环境之间的关系提供了证据。
|
图 4 在25℃、0.1MPa的有限水体及沉积物环境下时间的对数与草莓状黄铁矿粒径关系图(据Rickard,2019) Fig. 4 Logarithm of time verse framboid size for limiting conditions for water column and sediment at 25℃ and 0.1 MPa (after Rickard, 2019) |
尽管草莓状黄铁矿的有机成因和无机成因机制均有理论与实验的支撑,也有相应的假说为学者提出,但是如何严格界定有机和无机成因机制较为模糊,对两种机制下形成的草莓状黄铁矿的根本区别尚未进行深入研究。
3 草莓状黄铁矿的特征和古氧化-还原环境的反演 3.1 反演古氧化-还原环境的原理Ohfuji and Rickard(2005)实验研究表明:胶黄铁矿的形成是草莓状黄铁矿形成中一个非常重要的中间产物。在自然条件下,单硫化铁(FeS)是在还原环境下形成,而胶黄铁矿(Fe3S4)的形成在弱氧化条件下形成,在胶黄铁矿(Fe3S4)在向黄铁矿(FeS2)交代过程中,需要在还原条件下进行(Cutter et al., 1988;Muramoto et al., 1991)。草莓状黄铁矿作为一种间接沉积物,形成于氧化-还原界面附近,离开氧化-还原界面将不再生长(Raiswell, 1982;Canfield et al., 1994)。
根据水体含氧量的差异,沉积环境可以分为硫化/厌氧环境、缺氧环境、贫氧/次氧化环境和常氧环境(表 1)(Tyson et al., 1991)。不同氧化-还原环境下草莓状黄铁矿的形成环境、体系和阶段方面均存在不同,导致草莓状黄铁矿在粒径大小及形态、微晶大小及形态和硫同位素等方面存在明显的差异。
|
|
表 1 根据溶解氧划分的古氧化-还原环境(据Tyson and Pearson, 1991) Table 1 Classification of paleo-redox conditions based on dissolved oxygen (after Tyson and Pearson, 1991) |
这里需要讨论一下草莓状黄铁矿形成环境、体系及阶段的关系。硫化环境下草莓状黄铁矿形成于沉积物-水界面之上的水体中,形成过程中反应物(S源、Fe源)无限供给,为开放体系,对应于同沉积阶段(图 5a);氧化-贫氧环境下草莓状黄铁矿形成于沉积物-水界面之下的沉积物中,形成过程中反应物有限供给,为封闭体系,对应于成岩阶段初期(图 5b)(Love et al., 1966;Degens et al., 1972;Sawlowicz, 1993)。

|
图 5 草莓状黄铁矿在不同沉积环境、阶段及体系下形成的粒径分布特点和两种环境下形成的模式图 Fig. 5 The size distribution characteristics of framboidal pyrite formed in different sedimentary environments, stages and systems, and the model of formation in two environments |
硫化环境下形成的草莓状黄铁矿,物源主要来自水体,供给相对充足,在较短的时间内就可以形成,滞留时间相对较短,此外由于微晶相互间的磁性作用相互聚集,当微晶聚集到一定程度或吸附于悬浮颗粒之上,聚集体质量增加导致沉积(图 5a),形成的草莓状黄铁矿粒径相对较小且分布范围较窄(Raiswell, 1982;Wilkin, 1995;Wilkin et al., 1996);氧化-贫氧环境下形成草莓状黄铁矿,物源主要来自沉积物孔隙水体,供给相对的有限,形成时间相对较长,此外在硫酸盐还原带由于沉积物颗粒的相互支撑作用,微晶的聚集下沉不明显(图 5b),形成的草莓状黄铁矿粒径相对较大且分布范围较广(Raiswell, 1982;Wilkin, 1995;Wilkin et al., 1996)。两种环境下形成的草莓状黄铁矿的粒径分布均属于正态分布(Wilkin et al., 1996)。
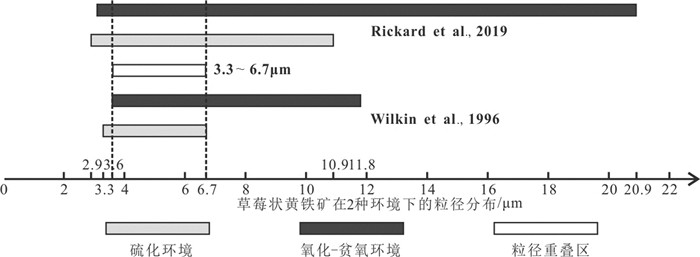
目前,利用草莓状黄铁矿粒径对古氧化-还原环境进行反演的方法主要有平均粒径法和最大粒径法(Wilkin et al., 1996;Wignall et al., 1998)。平均粒径法认为在硫化环境中形成的草莓状黄铁矿平均粒径范围(5.0±1.7 μm),粒径大于10 μm的约占4%;而氧化-贫氧环境中形成的草莓状黄铁矿平均粒径范围(7.7±4.1 μm),粒径大于10 μm占10%~50%;Rickard(2019)认为硫化环境下形成的草莓状黄铁矿粒径在2.9~10.9 μm,氧化-贫氧环境下形成的草莓状黄铁矿粒径为3.1~20.9 μm。Wilkin et al.(1996)和Rickard(2019)提出的草莓状黄铁矿粒径在硫化环境和氧化-贫氧环境的分布区间上存在着重叠,尤其在3.3~6.7 μm(图 6),这个粒径区间的草莓状黄铁矿在反演古氧化-还原环境时存在明显的不确定性。最大粒径法认为硫化环境形成的草莓状黄铁矿最大粒径一般小于20 μm,氧化环境中最大粒径一般大于20 μm(Wignall and Newton, 1998)。这里需要注意的是对粒径异常值的处理,异常值包括异常大或异常小值,两者可能反映了一次古氧化-还原环境的突变,不能盲目地删除。
|
图 6 草莓状黄铁矿粒径在硫化环境和氧化-贫氧环境下的分布及明显的重叠分布(数据来源于Wilkin et al., 1996和Rickard, 2019) Fig. 6 The size distribution and significant overlapping distribution of framboidal pyrite in euxinic conditions and oxic-dysoxic conditions (data from Wilkin et al., 1996 and Rickard, 2019) |
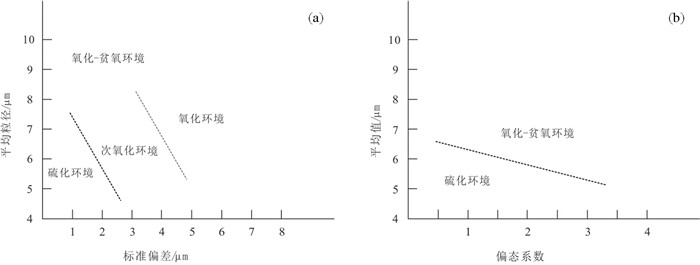
Wilkin et al.(1996)最早对现代海洋沉积物中草莓状黄铁矿粒径的平均值与标准偏差、偏态系数进行统计分析表明在硫化环境中,草莓状黄铁矿粒径的σ/X值基本恒定在0.34±0.02范围;而在氧化-贫氧环境中,草莓状黄铁矿粒径的σ/X值在0.55±0.15范围,认为在硫化环境,草莓状黄铁矿的粒径相对于氧化-贫氧环境变化较小(图 7a)。上述划分方案并没有涉及贫氧/次氧化和氧化环境的划分,常华进等(2009)结合老堡组硅质岩和Peru Margin次氧化环境下形成的草莓状黄铁矿数据(Wilkin et al., 1996),将氧化-贫氧环境进一步划分为次氧化和氧化两个区域(图 7a)。同样,也可以用草莓状黄铁矿的平均粒径与偏态系数对古氧化-还原环境进行反演(图 7b)。常晓琳等(2020)对扫描电镜下草莓状黄铁矿的粒径统计过程需要注意的事项进行了详细的论述,盒须图在粒径分布特征方面的应用也非常广泛。
|
图 7 草莓状黄铁矿的平均粒径与标准偏差(a)、偏态系数(b)图解(据Wilkin et al., 1996;常华进等,2009) Fig. 7 Plot of the mean vs. the standard deviation of the framboid size distributions (a), plot of the mean vs. the skewness of the framboid size distributions (b) (after Wilkin et al., 1996; Chang et al., 2009) |
Bond and Wignall(2010)结合前人与自己对黑海的研究,根据草莓状黄铁矿粒径分布将其形成环境分为硫化环境、厌氧环境、下部贫氧环境、上部贫氧环境和常氧环境5种,并对5种环境下草莓状黄铁矿粒径、含量、分布和沉积方面的特征进行总结(表 2)。
|
|
表 2 草莓状黄铁矿粒径特征与古氧化-还原环境及沉积特征总结(据Bond and Wignall, 2010) Table 2 Summary of characteristics used to define paleo-redox conditions during deposition(after Bond and Wignall, 2010) |
黄铁矿模拟实验中,不同的理化条件(例如Fe2+、硫化物、铁硫摩尔比、pH、Eh、氧化剂、杂质、温度等)下形成的黄铁矿呈不同的形态,主要有草莓状、假草莓状、充填型草莓状及自形晶等黄铁矿形态(Ohfuji et al., 2005; Lin et al., 2020)。Canfield et al.(1992)认为在早成岩阶段,草莓状黄铁矿是黄铁矿的主要形态,后期由于环境条件的变化有可能会进一步生长演化至自形晶,具体演化顺序可表示为球状→亚自形→含微晶自形态→自形态(图 8)(Merinero et al., 2008)。在活性铁含量低、有机碳含量高及酸性条件下,自形晶黄铁矿也可直接析出(Wignall et al., 1998;Ohfuji et al., 2005)。

|
图 8 草莓状黄铁矿形态演化(据Merinero et al., 2008) Fig. 8 Textural evolution of framboidal pyrite (after Merinero et al., 2008) |
Raiswell(1982)、Berner and Raiswell(1983)研究认为在氧化-贫氧环境下,由于沉积物与上覆水体循环受限,形成草莓状黄铁矿的S2-、Fe2+、溶解态的多硫化物等被认为是有限的,这种环境下更易于形成自形黄铁矿;Wilkin et al.(1996)研究发现尽管不同环境下黄铁矿的形态均以草莓状为主且发育少量的自形黄铁矿,但这种现象在硫化环境为主的黑海沉积物中尤其显著。这两个研究表明,随着硫化环境向氧化-贫氧环境的过渡,草莓状黄铁矿占比逐渐降低,而自形黄铁矿占比逐渐增大,原因可能与环境变化致使黄铁矿结晶-成核的动力学发生变化有关。
3.4 草莓状黄铁矿的微晶大小对古氧化-还原环境的反演草莓状黄铁矿微晶的等维及等形特征表明在聚集形成草莓状黄铁矿之前,存在一个微晶成核和生长的初始阶段(Taylor, 1982;Wilkin, 1995),从这个意义上讲,草莓状黄铁矿的成核和平均线性生长速率分别与其微晶的形成和聚集速率有关。
草莓状黄铁矿微晶生长速率的研究有稳定与非稳定状态两种假设:McCabe定律认为:微晶生长速率不随晶体直径、时间变化而变化,是溶液过饱和度的函数,是一个稳定态的假设,反映了微晶形成是一个连续结晶过程。此假设应用在CSD模型中,简化了一般的总体平衡方程(Wilkin et al., 1996),可以表示为:
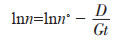
|
式中n表示单位体积溶液在给定直径范围内的晶体数量;no表示成核密度或成核初期的填充密度;D表示晶体直径;G表示生长速率;t表示生长时间。而非稳定状态假设认为微晶的生长速率与表面积成正比,即生长速率是随着晶体直径发生变化的,是一个非稳定的状态,反映了微晶的形成是一个分批次的过程(Randolf et al., 1971)。
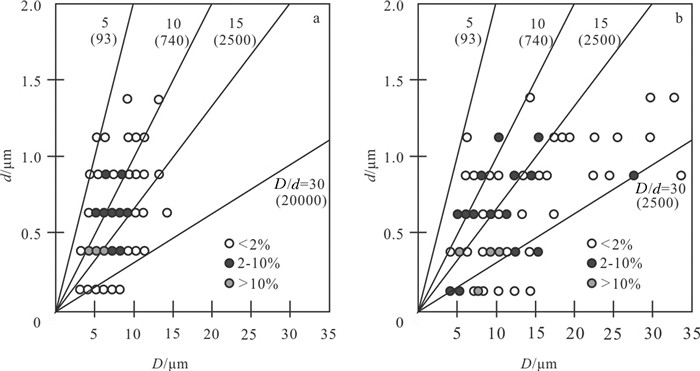
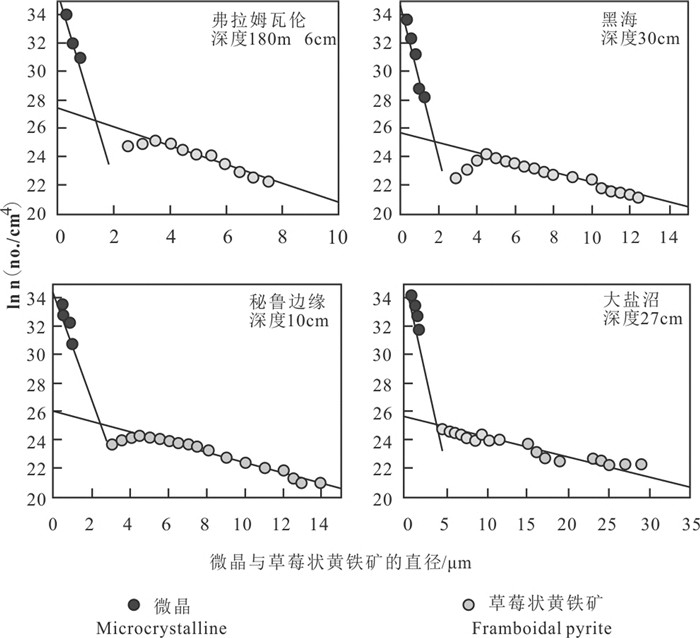
已有研究表明草莓状黄铁矿和微晶之间在直径方面存在良好的正相关性(图 9)(Sawlowicz, 1993;Wilkin et al., 1996;韦雪梅, 2017),但是微晶生长的速率和草莓状黄铁矿聚集速率存在差异(图 10)(Wilkin et al., 1996)。这些研究表明控制微晶和草莓状黄铁矿的形态演化、生长、聚集因素是不一致的,但是尚不清楚具体的控制因素。
|
图 9 黑海沉积物(a)和大盐沼沉积物(b)中草莓状黄铁矿粒径(D)与微晶直径(d)的关系(据Wilkin et al., 1996) Fig. 9 Relationships between framboid diameters (D) and microcrystal diameters (d) in Black Sea (a) sediments (30 cm) and Great Salt Marsh (b) sediments (27 cm)(after Wilkin et al., 1996) |
|
图 10 四个地点微晶与草莓状粒径分布图(据Wilkin et al., 1996) Fig. 10 Microcrystal and framboid size distribution plots of four samples (after Wilkin et al., 1996) |
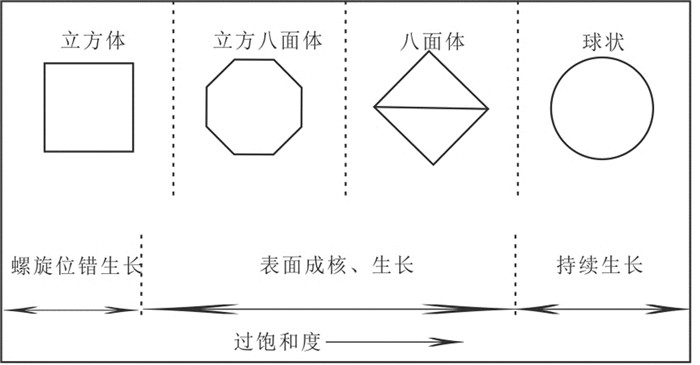
草莓状黄铁矿中微晶主要有四面体、立方体、八面体、五角十二面体及似球状等形态(Sweeney et al., 1973;Wilkin et al., 1997a;Butler et al., 2000)。微晶的形态不仅受控于晶体结构及晶体缺陷,更重要的是微晶的生长环境(黄铁矿浓度、pH、Eh、温度、杂质等)(Hartman et al., 1955;Tauson et al., 1993;Wang et al., 1996)。Wang and Morse(1996)的实验过程中观察到微晶呈立方体形态→十四面体(八面体)形态→球形的演化趋势(图 11),认为是晶体的生长形态偏离了平衡态,动力学机制变得更为重要,而溶液pH、离子强度和反应物的相对浓度等因素似乎并不显著,温度和杂质对微晶形态的影响目前还不清楚。
|
图 11 室温下一种黄铁矿微晶形态的演化和生长示意图(据Wang and Morse, 1996) Fig. 11 A schematic illustration of the changes of pyrite morphology and growth mechanism with the degree of supersaturation at room temperature (after Wang and Morse, 1996) |
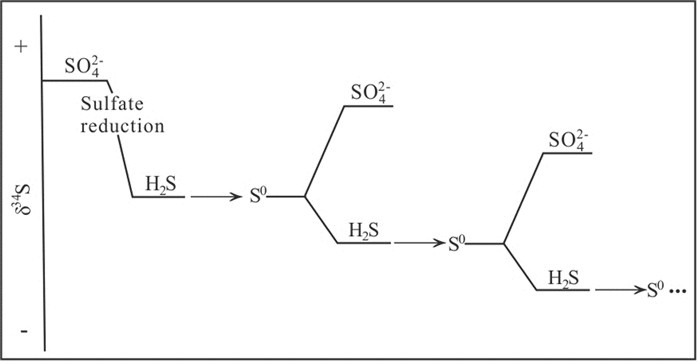
黄铁矿中硫同位素的差异是在生物或非生物过程中,对不同环境、不同分馏作用的综合反映。在硫同位素分馏过程中,硫酸盐首先进行32S轻同位素的分馏,而后进行34S重同位素的分馏,遵循质量相关分馏(Goldhaber et al., 1975;Gomes et al., 2018)。Canfield and Thamdrup(1994)的实验表明,硫同位素分馏主要是由硫酸盐还原菌还原硫酸盐过程产生的分馏和中间价态的硫化物发生歧化反应时产生的分馏综合作用的结果,提出了中间价态的硫在歧化反应过程中的循环氧化的模式(图 12)。
|
图 12 歧化反应过程中硫化物重复氧化为S0的模式图(据Canfield and Thamdrup, 1994) Fig. 12 A generalized scheme showing how repeated sulfide oxidation to S0 followed by disproportionation (after Canfield and Thamdrup, 1994) |
硫同位素的分馏受控于细菌种属、可用碳源、反应速率及水体化学条件等环境(张伟等, 2007),差异可以用硫同位素分馏程度(△δ34S)来衡量(Canfield et al., 2000),即:
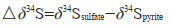
|
硫化环境中由于草莓状黄铁矿形成于沉积物-水界面之上的水体中,物源在形成草莓状黄铁矿的过程中无限供给,形成的草莓状黄铁矿中富集32S,亏损34S,草莓状黄铁矿中δ34Spyrite值相对负漂。如现代黑海沉积物中δ34Spyrite值可达-40‰ ~-55‰,分馏程度达70‰;氧化-贫氧环境中草莓状黄铁矿形成于沉积物-水界面之下,物源在形成草莓状黄铁矿的过程中有限供给,硫同位素在分馏过程中可使硫源中32S耗尽,形成的草莓状黄铁矿中δ34Spyrite值相对正漂。Habaicht and Canfield(1997)以及Habaicht et al.(2002)认为在开放体系中硫同位素(△δ34S)分馏程度大于22‰,封闭体系中硫同位素(△δ34S)分馏程度小于22‰。目前硫同位素的测定方法主要采用Canfield et al.(1986)提出的铬还原法。
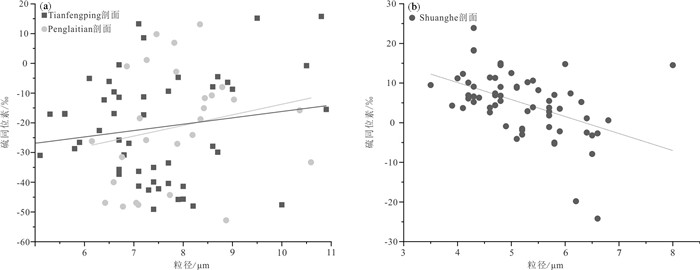
结合上述草莓状黄铁矿粒径与硫同位素对古氧化-还原环境的响应,可以得出这样一个结论:沉积作用形成的草莓状黄铁矿随着由硫化环境向氧化-贫氧环境的过渡,粒径逐渐增大,硫同位素相对正漂,粒径与硫同位素具有良好的正相关性。然而这种正相关性表现并不明显,甚至表现为弱负相关性(图 13)(Wei et al., 2016;Zou et al., 2018),究其原因在于硫同位素的测定方法,铬还原法测定的硫同位素,其值并非完全来自草莓状黄铁矿,还包括其他形态的黄铁矿以及其他硫化物,是样品硫同位素组成的平均值,这必然导致硫同位素与草莓状黄铁矿粒径之间的相关性与上述结论不符,例如同一块样品的全岩硫同位素与大颗粒黄铁矿硫同位素之间就存在差异(胡永亮等, 2020)。
|
图 13 草莓状黄铁矿粒径与硫同位素关系图 (a, 数据来源于韦恒叶等,2016;b, 数据来源于邹才能等,2018) Fig. 13 The relationships between the size and sulfur isotope of framboidal pyrite (a, data from Wei Hengye et al., 2016; b, data from Zou Caineng et al., 2018) |
为准确反映草莓状黄铁矿硫同位值,需要对草莓状黄铁矿进行原位硫同位素测试,目前最常用的分析方法有LA-MC-ICPMS和SIMS两种方法,主要用于3个方面的研究(Lin et al., 2016;Magnall et al., 2016;范宏瑞等, 2018;高永伟等,2019;周伶俐等,2019;Bryant et al., 2020;Huang et al., 2020;刘斌等, 2020;肖凡等2020;Nozaki et al., 2020;Sun et al., 2020;Xu et al., 2020;Zheng et al., 2020):(1)金属矿床的成因过程中对硫化物中微量元素富集的影响;(2)甲烷厌氧氧化与微生物硫酸盐还原过程对硫同位素变化的影响;(3)不同硫源对硫化物的相对贡献及系统硫循环的研究。
Meyer et al.(2019)用SIME和SEM分别测定了草莓状黄铁矿的硫同位素(δ34S)和粒径,结果表明两者没有明显的相关性。截止目前,尚未有其他学者以草莓状黄铁矿为研究对象,用LA-MC-ICPMS和SIMS两种方法代替铬还原法并结合SEM,对区域古氧化-还原环境及硫同位素与粒径之间的关系进行研究。
综上讨论,目前在使用草莓状黄铁矿反演区域古氧化-还原环境时,存在两方面的问题:草莓状黄铁矿粒径在3.3~6.7 μm明显的重叠和铬还原法表征草莓状黄铁矿硫同位素的准确性问题,仅用草莓状黄铁矿这一指标反演区域古氧化-还原环境时存在一定的局限性。为了进行高分辨古氧化-还原环境的重建,除需进行沉积作用下草莓状黄铁矿原位硫同位素测试外,尚需结合其他古氧化-还原指标进行综合判断,常用的指标有氧化-还原敏感微量元素(Mo、V、U等)、铁组分分析、同位素(δ98Mo、δ238U)、古岩相和古生物(笔石类、腕足类、有孔虫等)(Chen et al., 2004;Yan et al., 2012;朱祥坤等, 2013)等。
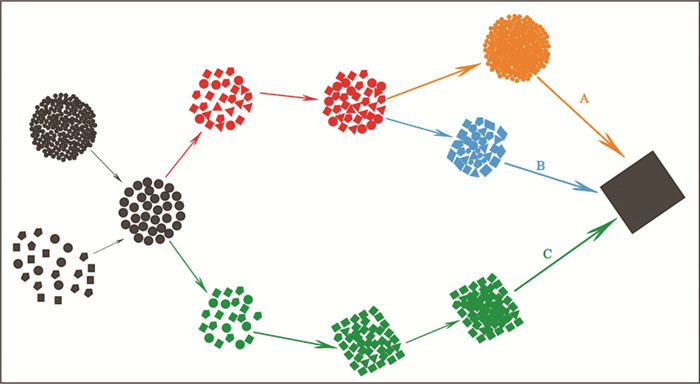
5 草莓状黄铁矿后期的演化草莓状黄铁矿的稳定性是有限的,在环境变化的情况下,是可以向自形黄铁矿演化的(Berner, 1967;Raiswell, 1982;Sawlowicz, 1993;Merinero et al., 2008)。Sawlowicz(1993)提出3种演化模式(图 14):(1)草莓状黄铁矿中微晶持续生长产生融合作用,可以填补内部空隙空间,形成块状黄铁矿小球,这些球状物可能进一步演化为自形黄铁矿(模式A)。(2)草莓状黄铁矿中微晶紧密排列时,外层发育一层细长的晶粒,通常只有一颗粒厚(Love et al., 1973),进一步生长可以使这种结构转变为自形晶(模式B)。(3)草莓状黄铁矿内部物质具有足够的塑性以至于可以移动时,将直接通过多边形草莓状向自形的生长(模式C)。
|
图 14 草莓状黄铁矿向自形黄铁矿演化的3种模式(据Sawlowicz,1993) (A、B、C代表 3种不同的演化模式) Fig. 14 Three evolutionary modelss for the formation of euhedral pyrite via framboids (after Sawlowicz, 1993) (A, B, C represent three different evolutionary models) |
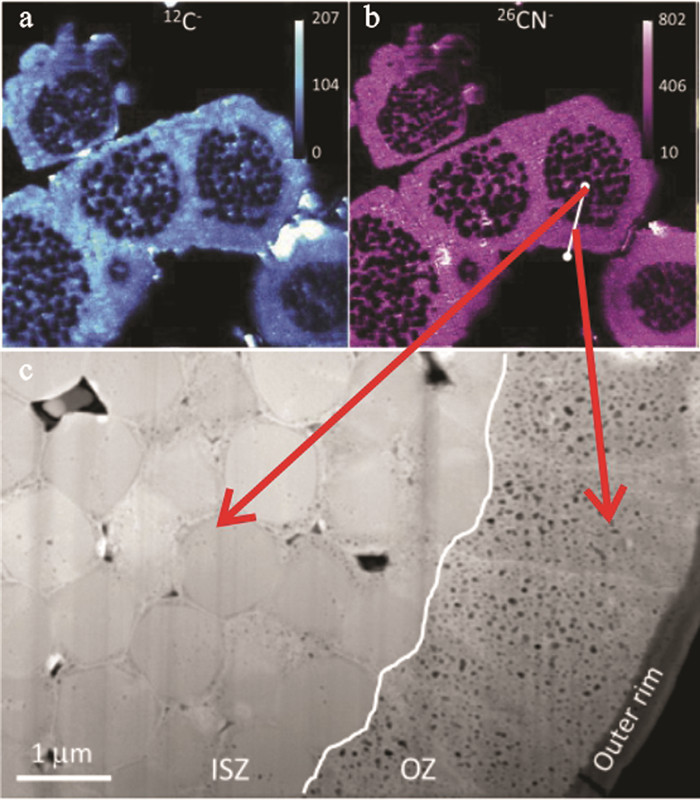
草莓状黄铁矿的二次生长现象在页岩中较为普遍,最明显的特征是在原来草莓状黄铁矿外围形成一圈呈放射状的外环结构(Outer rim)(图 15)(Wacey et al., 2015)。二次生长的原因可能是由于生物扰动引起沉积物与上覆水体的重新接触,导致草莓状黄铁矿与Fe2+、HS-及Sx-等离子再次相互接触所致(Wilkin et al., 1996)。
|
图 15 草莓状黄铁矿的二次生长对结构的改变(据Wacey et al., 2015) (ISZ(inner spheroidal zone)表示草莓状黄铁矿内部微晶带,OZ(overgrowth zone)表示草莓状黄铁矿外部二次生长带;图b中的白线为c图透射电子显微镜分析的位置) Fig. 15 Modification of framboidal pyrite structure by secondary growths (after Wacey et al., 2015) (ISZ represent inner spheroidal zone and OZ represent overgrowth zone of framboidal pyrite; White line in b shows approximate location of transmission election microscopy sample analyzed in Fig.c) |
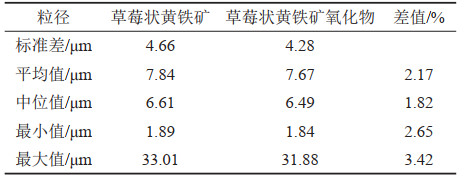
成岩后期的氧化作用也会不同程度地对岩层中草莓状黄铁矿的化学成分产生影响。黄元耕等(2018)在对塔西北地区大湾沟剖面、Guryul剖面和Barus Spur剖面的草莓状黄铁矿进行观察时发现很多草莓状黄铁矿表面呈绒毛状,分析认为这种表面呈绒毛状的铁氧化物来自草莓状黄铁矿的后期氧化,对表面氧化和未氧化的草莓状黄铁矿进行粒径统计分析,认为二者在标准差、平均值、中位值、最大值之间的差值≤3.42%(表 3),粒径分布特征极其相似(黄元耕, 2018; Huang et al., 2019)。尽管草莓状黄铁矿在后期氧化作用下,表面化学成分会发生变化,但依旧能保持原始草莓状黄铁矿的粒径分布特征,可以作为反演古氧化-还原环境的指标。
|
|
表 3 草莓状黄铁矿与草莓状黄铁矿氧化物粒径数据对比表(据黄元耕,2018) Table 3 Comparison table of oxide particle size data of framboidal pyrite and framboidal pyrite (after Huang Yuangeng, 2018) |
草莓状黄铁矿在反演古氧化-还原环境、硫循环及生命演化等方面具有非常重要的潜力,是研究地球重大地质事件的媒介之一,自发现以来一直都是研究的热点。尽管国内外学者对草莓状黄铁矿的成因机制、实验模拟、古氧化-还原反演及后期演化等方面进行了大量的研究,取得丰富的理论成果,但是以下3个方面尚需进一步研究。
6.1 提高模拟实验与地质环境的相似度在草莓状黄铁矿的模拟实验中,实验模拟条件与地质环境之间存在较大的差异。例如模拟实验的温度多高于60℃,而同沉积期和成岩阶段早期,温度尚未达到60℃;模拟实验均未考虑压力的效应,没有从成岩的角度去探讨草莓状黄铁矿的形成机制,不能精确定义草莓状黄铁矿的形成,没有建立具有普遍形成意义的草莓状黄铁矿成因体系。下一步模拟实验的重点应尽可能考虑地质环境因素,缩小模拟实验与地质环境的差距。
6.2 完善草莓状黄铁矿的理论体系尽管已初步建立了草莓状黄铁矿的无机和有机2种成因机制理论体系,但是一些基本问题尚未得到很好的解释。例如草莓状黄铁矿的有机与无机成因如何界定以及2种成因机制下形成的草莓状黄铁矿的根本区别;草莓状黄铁矿粒径与微晶生长理论及其演化序列;草莓状黄铁矿硫同位素原位测试及与粒径对古氧化-还原环境的表征。下一步工作尚需对草莓状黄铁矿相关理论体系进行完善。
6.3 加强草莓状黄铁矿在多学科之间的应用未来学科的研究将不再是局限于单一的学科研究,而是多学科之间的交叉研究。草莓状黄铁矿作为连接生物与环境的媒介之一,从前寒武纪到第四纪,伴随着生物不断演化、环境不断变迁而持续形成,通过草莓状黄铁矿来挖掘古生物和古环境信息,对我们了解地球生物学具有重要意义。大量研究表明富有机质页岩中TOC的含量与草莓状黄铁矿的发育有良好的正相关性,TOC是传统烃源岩评价的一个重要参数,但是由于TOC是烃源岩中残余有机碳总量,评价过程中存在多解性,草莓状黄铁矿相对稳定的性质和与TOC良好的正相关性能否作为烃源岩评价的一种指标亟需研究。草莓状黄铁矿在粒径、硫同位素等方面与形成环境具有紧密的关系,而环境又与沉积相带有密切的关系,在沉积相带相关研究中,草莓状黄铁矿是否可以作为一种指标进行相带划分等研究,尚需进一步研究。
7 结论前人在草莓状黄铁矿的形成机制、反演古氧化-还原环境和后期演化方面进行大量的实验和应用研究,取得重要成果。随着问题研究的深入和学科交叉的扩展,以下关于草莓状黄铁矿的问题尚需进一步研究:
(1)仅以草莓状黄铁矿反演区域古氧化-还原环境时存在一定的局限性,需结合其他氧化-还原指标进行综合判断。原位硫同位素测试技术代替铬还原法并结合粒径分布特征,对反演区域古氧化-还原环境及硫同位素与粒径之间的关系尚需进一步研究。
(2)草莓状黄铁矿在后期由于环境的改变会以不同演化路径向自形黄铁矿演化。尽管后期受氧化作用的影响,草莓状黄铁矿表面的化学成分会发生变化,但粒径分布依然保留原始特征,具有氧化-还原环境指示意义。
(3)草莓状黄铁矿在模拟实验与地质环境的相似度的提高、理论体系的完善和多学科交叉之间的应用加强方面仍然存在一些问题缺乏深入研究,尚需进一步研究。
致谢:匿名审稿老师和中国石油勘探开发研究院的郭海莉老师对文章内容、结构等方面提出宝贵的修改意见,在此表示衷心的感谢!
Berner R A. 1967. Thermodynamic stability of sedimentary iron sulfides[J]. American Journal of Science, 265: 773-785. DOI:10.2475/ajs.265.9.773 |
Berner R A. 1969. Migration of iron and sulfur within anaerobic sediments during early diagenesis[J]. American Journal of Science, 267(1): 19-42. DOI:10.2475/ajs.267.1.19 |
Berner R A, Raiswell R. 1983. Burial of organic carbon and pyrite sulfur in sediments over phanerozoic time A new theory[J]. Geochimica et Cosmochimica Acta, 47(5): 855-862. DOI:10.1016/0016-7037(83)90151-5 |
Berner R A. 1984. Sedimentary pyrite formation: An update[J]. Geochimica et Cosmochimica Acta, 48(4): 605-615. DOI:10.1016/0016-7037(84)90089-9 |
Bond D P G, Wignall P B W. 2010. Pyrite framboid study of marine Permian-Triassic boundary sections: A complex anoxic event and its relationship to contemporaneous mass extinction[J]. Geological Society of America Bulletin, 122(7-8): 1265-1279. DOI:10.1130/B30042.1 |
Bryant R N, Jones C, Raven M R, Owens J D, Fike D A. 2020. Shifting modes of iron sulfidization at the onset of OAE-2 drive regional shifts in pyrite δ34S records[J]. Chemical Geology, 553: 119808. DOI:10.1016/j.chemgeo.2020.119808 |
Butler I B, Rickard D. 2000. Framboidal pyrite formation via the oxidation of iron (II) monosulfide by hydrogen sulphide[J]. Geochimica et Cosmochimica Acta, 64(15): 2665-2672. DOI:10.1016/S0016-7037(00)00387-2 |
Canfield D E, Raiswell R, Westrich J T, Reaves C M, Berner R A. 1986. The use of chromium reduction in the analysis of reduced inorganic sulfur in sediments and shales[J]. Chemical Geology, 54(1/2): 149-155. |
Canfield D E, Thamdrup B. 1994. The production of 34S-depleted sulfide during bacterial disproportionation of elemental sulfur[J]. Science, 266: 1973-1975. DOI:10.1126/science.11540246 |
Canfield D E, Habicht K S, Thamdrup B. 2000. The Archean sulfur cycle and the early history of atmospheric oxygen[J]. Science, 288: 658-661. DOI:10.1126/science.288.5466.658 |
Chang Huajin, Chu Xuelei, Feng Lianjun, Huang Jing. 2009. Framboidal pyrites in cherts of the Laobao Formation, South China: Evidence for anoxic deep ocean in the terminal Ediacaran[J]. Acta Petrologica Sinica, 25(4): 1001-1007 (in Chinese with English abstract). |
Chang Xiaolin, Huang Yuangen, Chen Zhongqiang, Hou Mingcai. 2020. The microscopic analysis of pyrite framboids and application in paleo-oceanography[J]. Acta Sedimentologica Sinica, 38(1): 150-165 (in Chinese with English abstract). |
Chen X, Rong J Y, Li A, Boucot J. 2004. Facies patterns and geography of the Yangtze region, South China, through the Ordovician and Silurian transition[J]. Palaeogeography, Palaeoclimatology, Palaeoecology, 204(3/4): 353-372. |
Cutter G A, Velinsky D J. 1988. Temporal variations of sedimentary sulfur in a Delaware salt marsh[J]. Marine Chemistry, 23: 311-327. DOI:10.1016/0304-4203(88)90101-6 |
Degens E T, Okada H, Honjo S, Hathaway J C. 1972. Microcrystalline sphalerite in resin globules suspended in Lake Kivu, East Africa[J]. Mineralium Deposita, 7(1): 1-12. |
Donald R, Southam G. 1999. Low temperature anaerobic bacterial diagenesis of ferrous monosulfide to pyrite[J]. Geochimica et Cosmochimica Acta, 63: 2019-2023. DOI:10.1016/S0016-7037(99)00140-4 |
England B M, Ostwald J. 1993. Framboid-derived structures in some Tasman fold belt base-metal sulphide deposits, New South Wales, Australia[J]. Ore Geology Reviews, 7(5): 381-412. DOI:10.1016/0169-1368(93)90002-G |
Fan Hongrui, Li Xinghui, Zuo Yabin, Chen Lei, Liu Wei, Hu Fangfang, Feng Kai. 2018. In-situ LA-(MC)-ICPMS and (Nano) SIMS trace elements and sulfur isotope analyses on sulfides and application to confine metallogenic process of ore deposit[J]. Acta Petrologica Sinica, 34(12): 3479-3496 (in Chinese with English abstract). |
Farina M, Esquivel D, Henrique G P, Barros L D. 1990. Magnetic iron-sulphur crystals from a magnetotactic microorganism[J]. Nature, 343: 256-258. DOI:10.1038/343256a0 |
Farquhar J, Bao H, Thiemens M. 2000. Atmospheric influence of Earth's earliest sulfur cycle[J]. Science, 289(5480): 756-759. DOI:10.1126/science.289.5480.756 |
Farquhar J, Savarino J, Airieau S, Mark H, Thiemens M H. 2001. Observation of wavelength-sensitive mass-independent sulfur isotope effects during SO2 photolysis: Implications for the early atmosphere[J]. Journal of Geophysical Research: Planets, 106(E12): 32829-32839. DOI:10.1029/2000JE001437 |
Farrand M. 1970. Framboidal sulphides precipitated synthetically[J]. Mineralium Deposita, 5(3): 237-247. |
Gao Yongwei, Wang Zhihua, Li Weiliang, Zhang Zhenliang. 2019. A review of pyrite mineralogy research in hydrothermal gold deposits[J]. Northwestern Geology, 52(3): 58-69 (in Chinese with English abstract). |
Goldhaber M B, Kaplan I R. 1975. Controls and consequences of sulfate reduction rates in recent marine sediments[J]. Soil Sci., 119: 42-55. DOI:10.1097/00010694-197501000-00008 |
Gomes M L, Fike D A, Bergmann K D, Jones C, Knoll A H. 2018. Environmental insights from high-resolution (SIMS) sulfur isotope analyses of sulfides in Proterozoic microbialites with diverse mat textures[J]. Geobiology, 16(1): 17-34. DOI:10.1111/gbi.12265 |
Habicht K S, Canfield D E. 1997. Sulfur isotope fractionation during bacterial sulfate reduction in organic-rich sediments[J]. Geochimica et Cosmochimica Acta, 61(24): 5351-5361. DOI:10.1016/S0016-7037(97)00311-6 |
Habicht K S, Gade M, Thamdrup B, Berg P, Canfield D E. 2002. Calibration of sulfate levels in the archean ocean[J]. Science, 298(5602): 2372-2374. DOI:10.1126/science.1078265 |
Huang Fei, Gao Shang, Chen Lei, Su Limin, Li Yongli, Meng Lin, Liu Kaijun, Chai Chenwei, Qi Xinyi. 2020. Micro-texture and in situ sulfur isotope of pyrite from the Baiyunpu Pb-Zn deposit in central Hunan, South China: Implications for the growth mechanism of colloform pyrite aggregates[J]. Journal of Asian Earth Science, 193(15). |
Hartman P, Perdok W G. 1955. On the relations between structure and morphology of crystal1[J]. Acta Crystallographica(Section A), 8(1): 49-52. DOI:10.1107/S0365110X55000121 |
Horiuchi S, Wade H, Moori T. 1974. Morphology and imperfection of hydrothermally synthesized greigite (Fe3S4)[J]. Journal of Crystal Growth, 24: 624-626. |
Hu Yongliang, Wang wei, Zhou Chuanming. 2020. Morphologic and Isotopic Characteristics of Sedimentary Pyrite: A case study from deepwater facies, Ediacaran Lantian Formation in South China[J]. Acta Sedimentologica Sinica, 38(1): 138-149 (in Chinese with English abstract). |
Huang Y, Chen Z, Algeo T J, Zhao L, Baud A, Bhat G M. 2019. Two-stage marine anoxia and biotic response during the Permian-Triassic transition in Kashmir, northern India: Pyrite framboid evidence[J]. Global and Planetary Change, 172: 124-139. DOI:10.1016/j.gloplacha.2018.10.002 |
Kalliokoski J, Cathles L. 1969. Morphology, mode of formation, and diagenetic changes in framboids[J]. Bulletin of the Geological Society of Finland, 41: 125-133. DOI:10.17741/bgsf/41.014 |
Konhauser K O. 1997. Bacterialiron biomineralisation in nature[J]. FEMS Micrology Review, 20: 315-326. DOI:10.1111/j.1574-6976.1997.tb00317.x |
Lin M, Huang F, Wang X Q, Gao W Y, Zhang B M, Song D, Li G L, Zhang B Y. 2020. An experimental study of the morphological evolution of pyrite under hydrothermal conditions and its implications[J]. Journal of Geochemical Exploration, 219. |
Lin Z, Sun X, Peckmann J, Lu Y, Xu L, Strauss H, Zhou H, Gong J, Lu H, Teichert B M A. 2016. How sulfate-driven anaerobic oxidation of methane affects the sulfur isotopic composition of pyrite: A SIMS study from the South China Sea[J]. Chemical Geology, 440: 26-41. DOI:10.1016/j.chemgeo.2016.07.007 |
Liu Bin, Chen Weifeng, Fang Qichun, Tang Xiangsheng, Mao Yufeng, Sun Liqiang, Gao Shuang, Yan Yongjie, Wei Xin, Ling Hongfei. 2020. Study on in-situ sulfur isotope compositions of sulfides: Implication for the source of Pb-Zn mineralized body of Niutoushan in the Xiangshan Area[J]. Earth Science, 45(2): 389-399 (in Chinese with English abstract). |
Liu Dameng, Yang Qi, Zhou Chunguang, Tang Dazhen, Kang Xidong. 1999. Occurrence and geological gensis of pyrite in Late Paleozoic coals in north china[J]. Geochimica, 28(4): 340-350 (in Chinese with English abstract). |
Love L G. 1957. Mircro-organisms and the presence of syngenetic pyrite[J]. Quarterly Journal of the Geological Society, 113: 429-440. DOI:10.1144/GSL.JGS.1957.113.01-04.18 |
Love L G, Amstutz G C. 1966. Review of microscopic pyrite from the Devonian chattanooga shale and rammelserg banderz[J]. Fortschr Mineral, 43: 273-309. |
Love L G, Brockley H. 1973. Peripheral radial texture in framboids of polyframboidal pyrite[J]. Fortschr. Miner, 50: 264-269. |
Lowenstam H. 1981. Minerals formed by organisms[J]. Science, 211(4487): 1126-1131. DOI:10.1126/science.7008198 |
MacLean L C, Tyliszczak T, Gilbert P U, Zhou D, Pray T J, Onstott T C, Southam G. 2008. A high-resolution chemical and structural study of framboidal pyrite formed within a low-temperature bacterial biofilm[J]. Geobiology, 6(5): 471-480. DOI:10.1111/j.1472-4669.2008.00174.x |
Magnall J M, Gleeson S A, Stern R A, Newton R J, Poulton S W, Paradis S. 2016. Open system sulphate reduction in a diagenetic environment-Isotopic analysis of barite (δ34S and δ18O) and pyrite (δ34S) from the Tom and Jason Late Devonian Zn-Pb-Ba deposits, Selwyn Basin, Canada[J]. Geochimica et Cosmochimica Acta, 180: 146-163. DOI:10.1016/j.gca.2016.02.015 |
Merinero R, Lunar R, Frias J M, Somoza L, Diaz-del-Rio V d. 2008. Iron oxyhydroxide and sulphide mineralization in hydrocarbon seep-related carbonate submarine chimneys, Gulf of Cadiz (SW Iberian Peninsula)[J]. Marine and Petroleum Geology, 25(8): 706-713. DOI:10.1016/j.marpetgeo.2008.03.005 |
Meyer K M, Alonso R M, Morrissey S, Jones C. 2019. Sulfur Isotope Measurements of Framboidal Pyrites from the Sediments and Water Column of a Stratified Euxinic Lake[C]//American Geophysical Union.
|
Moore R A, Lieberman B S. 2009. Preservation of early and Middle Cambrian soft-bodied arthropods from the Pioche shale, Nevada, USA[J]. Palaeogeography, Palaeoclimatology, Palaeoecology, 277(1/2): 57-62. |
Morse J, Wang W Q. 1997. Pyrite formation under conditions approximating those in anoxic sediments: II.Influence of precursor iron minerals and organic matter[J]. Marine Chemistry, 57: 187-193. DOI:10.1016/S0304-4203(97)00050-9 |
Muramoto J Honjo A S B F, Hay B J, Howarth R W, Cisne J L. 1991. Sulfur, iron and organic carbon fluxes in the Black Sea: Sulfur isotopic evidence for origin of sulfur fluxes[J]. Deep Sea Research Part A. Oceanographic Research Papers, 38: S1151-S1187. DOI:10.1016/S0198-0149(10)80029-9 |
Nozaki T, Nagase T, Ushikubo T, Shimizu K, Ishibashi J i, the D/V Chikyu Expedition 909 Scientists. 2020. Microbial sulfate reduction plays an important role at the initial stage of subseafloor sulfide mineralization[J]. Geology, 49(2). DOI:10.1130/G47943.1 |
Ohfuji H D Rickard. 2005. Experimental syntheses of framboids-a review[J]. Earth-Science Reviews, 71(3/4): 147-170. |
Popa R, Kinkle B K, Badescu A. 2004. Pyrite framboids as biomarkers for Iron-Sulfur Systems[J]. Geomicrobiology, 21(3): 193-206. DOI:10.1080/01490450490275497 |
Raiswell R. 1982. Pyrite, texture isotopic composition and the availability of iron[J]. American Journal of Science, 282: 1244-1263. DOI:10.2475/ajs.282.8.1244 |
Raiswell R, Berner R A. 1985. Pyrite formation in euxinic and semi-euxinic sediments[J]. American Journal of Science, 285(8): 710-724. DOI:10.2475/ajs.285.8.710 |
Randolf A D, Larson W A. 1971. Theory of Particulate Processes. Analysis and Techniques of Continuous Crystallization[M]. Academic Press, New York and London.
|
Rickard D. 2019. How long does it take a pyrite framboid to form[J]. Earth & Planetary Science Letters, 513: 64-68. |
Rickard D. 2019. Sedimentary pyrite framboid size-frequency distributions: A meta-analysis[J]. Palaeogeography, Palaeoclimatology, Palaeoecology, 522: 62-75. DOI:10.1016/j.palaeo.2019.03.010 |
Rickard D T. 1970. The origin of framboids[J]. Lithos, 3(3): 269-293. DOI:10.1016/0024-4937(70)90079-4 |
Rust G W. 1935. Colloidal primary copper ores at Cornwall mines, Southeastern Missouri[J]. The Journal of Geology, 43(4): 398-426. DOI:10.1086/624318 |
Sawlowicz Z. 1993. Pyrite framboids and their development: A new conceptual mechanism[J]. Geologische Rundschau, 82(1): 148-156. DOI:10.1007/BF00563277 |
Sawlowicz Z. 1987. Framboidal pyrite from the metamorphic Radzimowice Schists of Stara Gora(Lower Silesia, Poland)[J]. Mineral Polon, 18: 57-67. |
Steinike K. 1963. A further remark on biogenic sulfides: Inorganic pyrite spheres[J]. Econimic Geology, 58(6): 998-1000. DOI:10.2113/gsecongeo.58.6.998 |
Sun G T, Zeng Q D, Zhou L L, Wang Y B, Chen P W. 2020. Trace element contents and in situ sulfur isotope analyses of pyrite in the Baiyun gold deposit, NE China: Implication for the genesis of intrusion-related gold deposits[J]. Ore Geology Reviews, 11810. |
Sweeney R E, Kaplan I R. 1973. Pyrite framboid formation laboratory synthesis and marine sediments[J]. Economic Geology, 68(5): 618-634. DOI:10.2113/gsecongeo.68.5.618 |
Tauson V L, Abramovich M G, Akimov V V, Scherbakov V A. 1993. Thermodynamics of real mineral crystals: Equilibriumcrystal shape and phase size effect[J]. Geochimica et Cosmochimica Acta, 57: 815-821. DOI:10.1016/0016-7037(93)90170-2 |
Taylor G R. 1982. A mechanism for framboid formation as illustrated by a volcanic exhalative sediment[J]. Mineralium Deposita, 17(1): 23-36. |
Tyson R V, Pearson T H. 1991. Modern and ancient continental shelf anoxia: An overview[J]. Geol. Soc. Spec. Pub., 58: 1-24. DOI:10.1144/GSL.SP.1991.058.01.01 |
Wacey D, Kilburn M R, Saunders M, Cliff J B, Kong C, Liu A G, Matthews J J, Brasier M D. 2015. Uncovering framboidal pyrite biogenicity using nano-scale C/Norg mapping[J]. Geology, 43(1): 27-30. DOI:10.1130/G36048.1 |
Wang Q, Morse J W. 1996. Pyrite formation under conditions approximating those in anoxic sediments I.Pathway and morphology[J]. Marine Chemistry, 52(2): 99-121. DOI:10.1016/0304-4203(95)00082-8 |
Wei H Y, Wei X M, Qiu Z, Song H Y, Guo S. 2016. Redox conditions across the G-L boundary in South China: Evidence from pyrite morphology and sulfur isotopic compositions[J]. Chemical Geology, 440: 1-14. DOI:10.1016/j.chemgeo.2016.07.009 |
Wignall P B, Newton R. 1998. Pyrite framboid diameter as a measure of oxygen deficiency in ancient mudrocks[J]. American Journal of Science, 298(7): 537-552. DOI:10.2475/ajs.298.7.537 |
Wilkin R T. 1995. Size Distribution in Sediments, Synthesis, and Formation Mechanism of Framboidal[D]. PhD. Dissertation. The Pennsylvania State Universty,
|
Wilkin R T, Barnes H L, Brantly S L. 1996. The size distribution of framboidal pyrite in modern sediments: An indicator of redox conditions[J]. Geochimica et Cosmochimica Acta, 60(20): 3897-3912. DOI:10.1016/0016-7037(96)00209-8 |
Wilkin R T, Barnes H L. 1997a. Formation processes of framboidal pyrite[J]. Geochimica et Cosmochimica Acta, 61(2): 323-339. DOI:10.1016/S0016-7037(96)00320-1 |
Xiao Fan, Ban Yizhong, Fan Feipeng, Xu Naicen, Mao Guangwu, Li Fengchun. 2020. Research on zircon U-Pb, S-Pb isotopes and trace elements of pyrite from the Dongji Au(Ag) deposit in Zhenghe County, Fujian Province[J]. Geology in China, 47(2): 375-393 (in Chinese with English abstract). |
Xu Nan, Wu Cailai, Li Shengrong, Xue Boqiang, He Xiang, Yu Yanlong, Liu Junzhuang. 2020. LA-ICP-MS in situ analyses of the pyrites in Dongyang gold deposit, Southeast China: Implications to the gold mineralization[J]. China Geology, 3: 230-246. |
Yan D, Chen D, Wang Q, Wang J. 2012. Predominance of stratified anoxic Yangtze Sea interrupted by short-term oxygenation during the Ordo-Silurian transition[J]. Chemical Geology, 291: 69-78. DOI:10.1016/j.chemgeo.2011.09.015 |
Yang R, He S, Wang X, Hu Q, Hu D, Yi J, Widory D. 2016. Paleo-ocean redox environments of the Upper Ordovician Wufeng and the first member in lower Silurian Longmaxi formations in the Jiaoshiba area, Sichuan Basin[J]. Canadian Journal of Earth Sciences, 53(4): 426-440. DOI:10.1139/cjes-2015-0210 |
Yang Xueying, Gong Yiming. 2011. Pyrite framboid: Indicator of environments and life[J]. Earth Science, 36(4): 643-658 (in Chinese with English abstract). |
Zhang Wei, Liu Congqiang, Liang Xiaobing. 2007. Biological function in sulfur isotope fractionation and environmental effect[J]. Acta Geochimica, 35(3): 223-227 (in Chinese with English abstract). |
Zheng J H, Shen P, Li C H. 2020. Ore genesis of Axi post-collisional epithermal gold deposit, western Tianshan, NW China: Constraints from U-Pb dating, Hf isotopes, and pyrite in situ sulfur isotopes[J]. Ore Geology Review, 117. DOI:10.1016/j.orgrorev.2019.103290 |
Zhou Lingli, Zeng Qingdong, Sun Guotao, Duan Xiaoxia. 2019. Laser Ablation-Inductively Coupled Plasma Mass Spectrometry (LA-ICPMS) elemental mapping and its applications in ore geology[J]. Acta Petrologica Sinica, 35(7): 1964-1978 (in Chinese with English abstract). DOI:10.18654/1000-0569/2019.07.02 |
Zhu Xiangkun, Wang Yue, Yan Bin, Li Jin, Dong Aiguo, Li Zhihong, Sun Jian. 2013. Developments of non-traditional stable isotope geochemistry[J]. Bulletin of Mineralogy, Petrology and Geochemistry, 32(6): 651-688 (in Chinese with English abstract). |
Zou C N, Zhen Q, W H Y, Dong D Z, Lu B. 2018. Euxinia caused the Late Ordovician extinction Evidence from pyrite morphology and pyritic sulfur isotopic composition in the Yangtze area, South China[J]. Palaeogeography, Palaeoclimatology, Palaeoecology, 511: 1-11. DOI:10.1016/j.palaeo.2017.11.033 |
常华进, 储雪蕾, 冯连君, 黄晶. 2009. 华南老堡组硅质岩中草莓状黄铁矿-埃迪卡拉纪末期深海缺氧的证据[J]. 岩石学报, 25(4): 1001-1007. |
常晓琳, 黄元耕, 陈中强, 侯明才. 2020. 沉积地层中草莓状黄铁矿分析方法及其在古海洋学上的应用[J]. 沉积学报, 1: 150-165. |
范宏瑞, 李兴辉, 左亚彬, 陈蕾, 刘尚, 胡芳芳, 冯凯. 2018. LA-(MC)-ICPMS和(Nano)SIMS硫化物微量元素和硫同位素原位分析与矿床形成的精细过程[J]. 岩石学报, 34(12): 3479-3496. |
胡永亮, 王伟, 周传明. 2020. 沉积地层中的黄铁矿形态及同位素特征初探——以华南埃迪卡拉纪深水相地层为例[J]. 沉积学报, 38(1): 138-149. |
黄元耕. 2018. 华南及新疆地区二叠纪至三叠纪海洋、陆地古群落模拟及海洋氧化还原环境变化研究[D]. 中国地质大学(武汉).
|
刘斌, 陈卫锋, 方启春, 唐湘生, 毛玉锋, 孙立强, 高爽, 严永杰, 魏欣, 凌洪飞. 2020. 相山西部牛头山铅锌矿化体成矿物质来源: 原位硫同位素的制约[J]. 地球科学, 45(2): 389-399. |
刘大猛, 杨起, 周春光, 康西栋. 1999. 华北晚古生代煤中黄铁矿赋存特征与地质成因研究[J]. 地球化学, 28(4): 340-351. DOI:10.3321/j.issn:0379-1726.1999.04.004 |
韦雪梅. 2017. 广西蓬莱滩GSSP剖面G-L界线黄铁矿形态特征及其氧化还原意义[D]. 东华理工大学.
|
肖凡, 班宜忠, 范飞鹏, 许乃岑, 毛光武, 李凤春. 2020. 福建政和县东际金(银)矿床黄铁矿微量元素和硫-铅同位素及锆石年龄研究[J]. 中国地质, 47(2): 375-393. |
杨雪英, 龚一鸣. 2011. 莓状黄铁矿: 环境与生命的示踪计[J]. 地球科学, 36(4): 643-658. |
张伟, 刘丛强, 梁小兵. 2007. 硫同位素分馏中的生物作用及其环境效应[J]. 地球与环境, 35(3): 223-227. |
周伶俐, 曾庆栋, 孙国涛, 段晓侠. 2019. LA-ICPMS原位微区面扫描分析技术及其矿床学应用实例[J]. 岩石学报, 35(7): 1964-1978. |
朱祥坤, 王跃, 闫斌, 李津, 董爱国, 李志红, 孙剑. 2013. 非传统稳定同位素地球化学的创建与发展[J]. 矿物岩石地球化学通报, 32: 651-688. |